Dalbavancin ist ein neues Lipoglycopeptid-Antibiotikum der zweiten Generation. Es gehört zur gleichen Klasse wie Vancomycin, das am häufigsten eingesetzte und eine der wenigen Behandlungsmöglichkeiten für Patienten, die mit Methicillin-resistentem Staphylococcus aureus (MRSA) infiziert sind. Handelsnamen sind Xydalba, Zeven, Dalvance. ATC-Codes ist J01XA04.
News zu Dalbavancin
- 14.10.2022 EU: Der CHMP der EMA empfiehlt die Erweiterung der Indikation wie folgt: Xydalba ist für die Behandlung von akuten bakteriellen Infektionen der Haut und der Hautstrukturen (ABSSSI) bei Erwachsenen und Kindern ab 3 Monaten indiziert
- 10.08.2016 EU-Genehmigung für Einzeldosis bei ABSSSI
- 01.03.2015 EU-Zulassung für Xydalba bei bakteriellen Haut- und Weichgewebeinfektionen
- 19.12.2014 Xydalba: EMA-Zulassungsempfehlung bei Hautinfektionen
- FDA genehmigt Dalvance bei Hautinfektionen
FDA genehmigt Dalvance bei Hautinfektionen
Die US Food and Drug Administration hat das Antibiotikum Dalvance (Markenname ist in Europa Xydalba – Wirkstoff ist Dalbavancin) zur Behandlung von Erwachsenen mit Hautinfektionen genehmigt.
Dalvance soll bei akuten bakteriellen Haut- und Hautstrukturinfektionen eingesetzt werden, die durch bestimmte Bakterien wie Staphylococcus aureus (einschließlich Methicillin-empfindlichen und Methicillin-resistenten Stämmen) und Streptococcus pyogenes verursacht werden. Die Behandlung wird intravenös verabreicht.
Wirksamkeit
Sicherheit und Wirksamkeit von Dalbavancin wurden in zwei klinischen Studien mit insgesamt 1.289 Erwachsenen mit Haut- und Hautstrukturinfektionen ausgewertet. Die Teilnehmer erhielten randomisiert Dalbavancin oder Vancomycin, ein anderes antibakterielles Medikament. Die Ergebnisse zeigten, dass Dalbavancin genauso wirksam wie Vancomycin bei der Behandlung von Haut- und Hautstrukturinfektionen war.
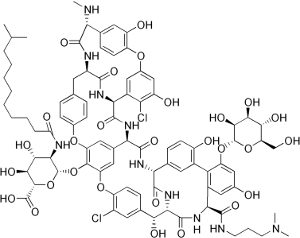
Der Wirkstoff von Xydalba ist Dalbavancin, ein antibakterielles Glycopeptid (J01XA04), das
die Zellwandsynthese bei anfälligen Gram-positiven Bakterien unterbricht.
Der Vorteil von Dalbavancin ist seine Fähigkeit gegen wichtige Gruppen von Gram-positiven Bakterien wirksam zu sein, einschließlich den Stämmen des Methicillin-resistenten Staphylococcus aureus (MRSA) und einigen S. aureus
mit einer verminderten Anfälligkeit gegenüber Glykopeptiden (GISA), sowie pathogenen Streptokokken.
Nebenwirkungen
Die in den klinischen Studien identifizierten häufigsten Nebenwirkungen waren Übelkeit, Kopfschmerzen und Durchfall. In den Versuchen zeigten mehr Teilnehmer der Dalvance-Gruppe Erhöhungen ihrer Leberenzymtests. Die Dalbavancin Gebrauchsanweisung empfiehlt Dosisanpassung bei Patienten mit eingeschränkter Nierenfunktion.
© arznei-news.de – Quelle: FDA, Mai 2014
Xydalba
EMA: Zulassungsempfehlung für Xydalba bei Hautinfektionen
19.12.2014 Der Ausschuss für Humanarzneimittel (CHMP) der Europäischen Arzneimittelagentur (EMA) empfiehlt, Xydalba, 500 mg, Pulver für ein Konzentrat zur Herstellung einer Infusionslösung für die Behandlung von akuten bakteriellen Haut- und Hautstrukturinfektionen (ABSSSI) bei Erwachsenen zuzulassen.
Der Antragsteller für das Arzneimittel ist die Firma Durata Therapeutics International BV.
Die am häufigsten auftretenden Nebenwirkungen sind Übelkeit, Durchfall und Kopfschmerzen.
Ein Pharmakovigilanz-Plan für Xydalba soll als Teil der Zulassung implementiert werden.
© arznei-news.de – Quelle: EMA, Dez. 2014
EU-Zulassung für Xydalba bei bakteriellen Haut- und Weichgewebeinfektionen
01.03.2015 Die Europäische Kommission hat Xydalba von der Firma Durata Therapeutics International B.V. mit dem Wirkstoff Dalbavancin bei bakteriellen Haut- und Weichgewebsinfektionen zugelassen.
Xydalba ist nun für die Behandlung von akuten bakteriellen Haut- und Hautstrukturinfektionen (ABSSSI) bei Erwachsenen indiziert.
Es ist den offiziellen Leitlinien für die adäquate Anwendung antibakterieller Wirkstoffe zu folgen.
© arznei-news.de – Quelle: European Commission, März 2015
EU-Genehmigung für Einzeldosis bei ABSSSI
10.08.2016 Die Europäische Arzneimittel-Agentur (EMA) hat Cardiome Pharmas Xydalba mit der aktiven Substanz Dalbavancin für die Verabreichung als Einzeldosis, 30 Minuten, 1500 mg Infusion (drei 500mg Phiolen) zur Behandlung von ABSSSI zugelassen.
Diese Einzeldosierung wurde zusätzlich zu der ursprünglich genehmigten Dosierung von 1000 mg (zwei 500 mg Phiolen) gefolgt von 500 mg eine Woche später (eine einzelne 500 mg Ampulle) zugelassen.
Cardiome Pharma geht davon aus, dass das Medikament in einigen der großen Gebieten unter Lizenz im vierten Quartal 2016 für Ärzte zur Verfügung stehen wird.
© arznei-news.de – Quelle: Cardiome Pharma, August 2016
