- Indikation
- 29.04.2016 EU-Zulassungsempfehlung – HIV-1
- 23.06.2016 EU-Zulassung zur Behandlung von HIV
- 24.07.2016 Primärziele in 2 HIV-Studien erreicht
- Erfahrungen, Erfahrungsberichte
EU-Zulassungsempfehlung – HIV-1
29.04.2016 Der Ausschuss für Humanarzneimittel der Europäischen Zulassungsbehörde (CHMP) empfiehlt die Zulassung von Odefsey Filmtabletten der Firma Gilead Sciences International Ltd zur Behandlung von HIV-1.
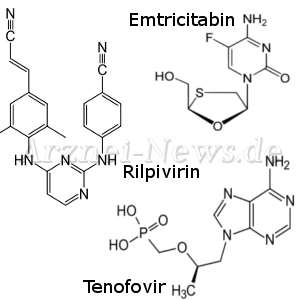 Odefsey ist eine Fixkombination aus drei Wirkstoffen: Rilprivirin, Emtricitabin und Tenofovir-Alafenamid (25 mg / 200 mg / 25 mg; ATC-Code: J05AR19).
Odefsey ist eine Fixkombination aus drei Wirkstoffen: Rilprivirin, Emtricitabin und Tenofovir-Alafenamid (25 mg / 200 mg / 25 mg; ATC-Code: J05AR19).
Emtricitabin und Tenofovir-Alafenamid sind Substrate und kompetitive Inhibitoren der HIV-Reverse Transkriptase. Nach der Phosphorylierung werden sie in die virale DNA-Kette eingebaut, wobei es zu einem Kettenabbruch kommt. Rilprivirins Aktivität wird durch nicht-kompetitive Hemmung der HIV-1-Reverse-Transkriptase vermittelt.
Der Nutzen des Medikaments ist seine Fähigkeit, ein antiretrovirales Ansprechen mit nur einer einmal täglich verabreichten einzelnen Tablette zu erreichen.
Indikation
Odefsey soll bei Zulassung für die Behandlung von Erwachsenen und Jugendlichen (12 Jahre und älter mit einem Körpergewicht von mindestens 35 kg) eingesetzt werden können, die mit dem humanen Immundefizienz-Virus 1 (HIV-1) infiziert wurden (ohne bekannte Mutationen, die mit der Resistenz mit der Klasse der Nicht-Nukleosid-Reverse-Transkriptase-Inhibitoren (NNRTI), Tenofovir oder Emtricitabin assoziiert sind) und mit einer Viruslast ≤ 100.000 HIV-1-RNA-Kopien / ml.
Die häufigsten Nebenwirkungen sind Übelkeit, Schlaflosigkeit und Schwindel.
© arznei-news.de – Quelle: EMA, April 2016
EU-Zulassung zur Behandlung von HIV
23.06.2016 Gilead Sciences hat bekanntgegeben, dass die Europäische Kommission die Marktzulassung für die einmal täglich einzunehmende Einzeltablettenkur (Single Tablet Regimen, STR) Odefsey (Emtricitabin 200 mg / Rilpivirin 25 mg / Tenofovir alafenamid 25 mg oder R / F / TAF) für die Behandlung von HIV-1-Infektion bei bestimmten Patienten erteilt hat.
Das Medikament ist in der Europäischen Union für die Behandlung von Erwachsenen und Jugendlichen (im Alter von 12 Jahren mit einem Körpergewicht von mindestens 35 kg) angezeigt (mehr zur Indikation).
Wirksamkeit
Die Genehmigung wird von einer Bioäquivalenz-Studie unterstützt, die zeigte, dass Odefsey ähnliche Arzneimittelkonzentrationen von Emtricitabin und TAF im Blut erreichen konnte wie Genvoya (Elvitegravir 150 mg / Cobicistat 150 mg / Emtricitabin 200 mg / Tenofovir alafenamide 10 mg; E / C / F / TAF) und ähnliche Wirkstoffkonzentrationen von Rilpivirin wie Edurant (Rilpivirin 25 mg).
Sicherheit, Wirksamkeit und Verträglichkeit von Odefsey wurden auch durch klinische Studien basierend auf einer Rilpivirin-Therapie (verabreicht als R + F / TDF oder Eviplera; Emtricitabin 200 mg / Rilpivirin 25 mg / Tenofovir Disoproxil Fumarat 245 mg) unterstützt und F / TAF- Therapie (verabreicht als Genvoya) bei Patienten mit HIV-1-Infektion.
Diese Patienten waren behandlungsnaive Erwachsene und Jugendliche, virussupprimierte Erwachsene, die von Protease-Inhibitor-basierten Regimen, NNRTI-basierten Regimen oder Integrase Strangtransfer-Inhibitor-basierten Regimen überwechselten, und virussupprimierte Erwachsene mit leichter bis mittelschwerer Niereninsuffizienz.
Wie bei allen Rilpivirin-haltigen Behandlungen, sollte Odefsey zusammen mit der Nahrung eingenommen werden.
© arznei-news.de – Quelle: Gilead Sciences, Juni 2016
Primärziele in 2 HIV-Studien erreicht
24.07.2016 Gilead Sciences hat bekanntgegeben, dass zwei Phase-3b-Switch-Studien zu Odefsey (Emtricitabin 200 mg / Rilpivirin 25 mg / Tenofovir-Alafenamid 25mg) und der Behandlung von HIV-1-Infektion ihre primären Ziele erreicht haben.
Die laufenden Studien wurden entwickelt, um Wirksamkeit und Sicherheit des Medikaments bei virussupprimierten erwachsenen Patienten nach dem Wechsel von Complera (Emtricitabin 200 mg / Rilpivirin 25 mg / Tenofovir Disoproxil Fumarat 300 mg) (Studie 1216) oder Atripla Regimen (Efavirenz 600mg / Emtricitabin 200 mg / Tenofovir Disoproxil Fumarat 300 mg) (Studie 1160) zu evaluieren.
Wirksamkeit in 1160 und 1216
Odefsey erreichte ähnliche Virussuppressionsraten wie die TDF-basierten Behandlungen in beiden Studien beim Anteil der Patienten mit HIV-1-RNA-Werten (Viruslast) <50 Kopien / ml.
In der 48. Woche konnte die Virussuppression der Odefsey einnehmenden Patienten bei 94 Prozent in Studie 1216 und 90 Prozent in Studie 1160 aufrechterhalten werden; dagegen bei 94 Prozent der Complera und 92 Prozent der Atripla einnehmenden Patienten.
Im Vergleich zu den TDF-basierten Therapien zeigte Odefsey statistisch signifikante Verbesserungen in der Knochenmineraldichte (BMD) an Hüfte und Wirbelsäule in beiden Studien. Zusätzlich begünstigte es statistisch die Verbesserungen bei insgesamter und tubulärer Proteinurie in beiden Studien.
Sicherheit in 1160 und 1216
Die Behandlungen wurden im Allgemeinen gut vertragen, und allgemeine Sicherheit und Abbruchraten aufgrund von unerwünschten Ereignisse waren vergleichbar in den beiden Studien.
Die am häufigsten berichteten unerwünschten Ereignisse für Odefsey waren:
- Infektionen der oberen Atemwege,
- Durchfall,
- Nasopharyngitis,
- Husten und
- Kopfschmerzen.
© arznei-news.de – Quelle: Gilead, Juli 2016
Schreiben Sie uns >> hier << über Ihre Erfahrungen und lesen Sie die Erfahrungsberichte / Kommentare zu diesem Medikament.
