- 18.04.2018 Chronische Immunthrombozytopenie: FDA-Zulassung
- 15.11.2019 EU: Primäre Immunthrombozytopenie – CHMP-Zulassungsempfehlung für Tavlesse
- 13.01.2020 Chronische Immunthrombozytopenie: EU-Zulassung für Tavlesse
- Weitere Infos (Wirksamkeit, Nebenwirkungen etc.), News zum Wirkstoff unter Fostamatinib
Chronische Immunthrombozytopenie: FDA-Zulassung
18.04.2018 Rigel Pharmaceuticals hat eine FDA-Zulassung für die Vermarktung von Tavalisse (Fostamatinib) zur Behandlung von Thrombozytopenie bei erwachsenen Patienten mit chronischer Immunthrombozytopenie (ITP) erhalten, die auf eine frühere Behandlung nicht angesprochen haben.
Chronische Immunthrombozytopenie
Chronische ITP ist eine seltene Autoimmunerkrankung, bei der das Immunsystem Blutplättchen zerstört, die für eine normale Blutgerinnung notwendig sind. Die Erkrankung ist schwierig zu behandeln, weil es unmöglich ist, vorherzusagen, wie die Menschen auf die verfügbaren Therapien reagieren werden.
Rund 50.000-60.000 Erwachsene leben in der mit primärem ITP, und viele sprechen nicht oder nicht mehr auf eine oder mehrere aktuelle Therapien an, stellte das Unternehmen fest und unterstrich den ungedeckten Bedarf in diesem Bereich.
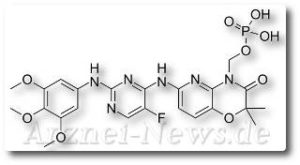
Fostamatinib Dinatriumhexahydrat
Tavalisse (Wirkstoff ist Fostamatinib Dinatriumhexahydrat), ein SYK-Inhibitor mit einem einzigartigen Wirkmechanismus, der die zugrundeliegende Autoimmunursache der Krankheit bekämpft, indem er die Zerstörung der Blutplättchen verhindert.
Nebenwirkungen
Schwere Nebenwirkungen in den ITP-Doppelblindstudien waren
- fieberhafte Neutropenie, Durchfall, Lungenentzündung und hypertensive Krise, die bei 1% der TAVALISSE-Patienten auftrat.
- Zusätzlich traten schwere Nebenwirkungen auf, darunter Dyspnoe und Bluthochdruck (beide 2%), Neutropenie, Arthralgie, Brustschmerzen, Durchfall, Schwindel, Nephrolithiasis, Schmerzen in den Extremitäten, Zahnschmerzen, Synkope und Hypoxie (alle 1%).
- Häufige Nebenwirkungen (≥5% und häufiger als Placebo) von FIT-1 und FIT-2: Durchfall, Bluthochdruck, Übelkeit, Schwindel, ALT und AST erhöht, Atemwegsinfektionen, Ausschlag, Bauchschmerzen, Müdigkeit, Brustschmerzen und Neutropenie.
Rigel plant, das Medikament nächsten Monat in den USA einzuführen.
© arznei-news.de – Quellenangabe: Rigel Pharmaceuticals
EU: Primäre Immunthrombozytopenie – CHMP-Zulassungsempfehlung für Tavlesse
15.11.2019 Der Ausschuss für Humanarzneimittel der Europäischen Zulassungsbehörde (CHMP) empfiehlt die Zulassung von Tavlesse (aktive Substanz ist Fostamatinib) der Firma Rigel Pharmaceuticals B.V. als 100-mg und 150-mg Filmtabletten für die Behandlung von Erwachsenen mit primärer Immunthrombozytopenie.
Fostamatinib blockiert die Milztyrosinkinase (SYK) und hemmt dadurch die Signaltransduktion von B-Zell-Rezeptoren und Fc-aktivierenden Rezeptoren, die eine Schlüsselrolle bei antikörpervermittelten Zellreaktionen spielen. Fostamatinib reduziert die durch Antikörper verursachte Zerstörung von Blutplättchen.
Tavlesse soll die Anzahl der Blutplättchen erhöhen und aufrechterhalten und das Blutungsrisiko reduzieren. Die häufigsten Nebenwirkungen sind Schwindel, Durchfall, Übelkeit, häufiger Stuhlgang, Bluthochdruck und Blutdruckanomalien sowie Anomalien im Leberfunktionstest.
Die vollständige Indikation bei Zulassung wäre: Tavlesse ist für die Behandlung der chronischen Immunthrombozytopenie (ITP) bei erwachsenen Patienten indiziert, die auf andere Behandlungen nicht ansprechen.
© arznei-news.de – Quelle: EMA
Kein Abo! (Schon ab 1,67€ für den Monat)
Chronische Immunthrombozytopenie: EU-Zulassung für Tavlesse
13.01.2020 Die Europäische Kommission hat am 13. Januar 2020 dem Medikament Tavlesse (Wirkstoff ist Fostamatinib) der Firma Rigel Pharmaceuticals B.V. die Zulassung für die Behandlung der chronischen Immunthrombozytopenie (ITP) bei erwachsenen Patienten, die gegenüber anderen Behandlungsarten therapieresistent sind, erteilt.
Der ATC-Code des Wirkstoffes ist: B02BX09.
© arznei-news.de – Quelle: EC, 2020