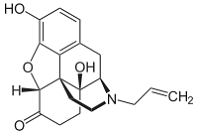
Naloxon (Markennamen Monopräparate: Nyxoid, Nexodal, Narcanti, Narcan, Prenoxad; Kombinationspräparate: Zubsolv) ist ein Medikament, das zur Hemmung der Wirkungen von Opioiden, insbesondere bei Überdosierung, eingesetzt wird.
Naloxon kann in Kombination mit dem Opioid in derselben Tablette verabreicht werden, um das Risiko von Missbrauch zu verringern. Wenn es intravenös verabreicht wird, wirkt es innerhalb von zwei Minuten, und wenn es in einen Muskel injiziert wird, innerhalb von fünf Minuten. Das Medikament kann auch über die Nase verabreicht werden. Die Wirkung hält etwa eine halbe Stunde bis zu einer Stunde an. Mehrere Dosen können erforderlich sein, da die Wirkungsdauer der meisten Opioide größer ist als die von Naloxon.
News zu Naloxon
- 20.08.2024 Naloxon bei Opioid- / Nicht-Opioid-bedingtem Herzstillstand. Zusammenhang zwischen Naloxon und den Behandlungsergebnissen bei außerklinischem Herz-Kreislaufstillstand
- 13.08.2024 Opioidabhängigkeit: Sicherheit von Buprenorphin + Naloxon in Schwangerschaft. Studie verglich Sicherheit einer In-Utero-Exposition mit Buprenorphin in Kombination mit Naloxon gegenüber Buprenorphin allein
- 09.02.2024 Naloxon bei Opioid-Überdosis. Vergleich der Verabreichung von 8-Milligramm und 4-Milligramm intranasalem Naloxon durch die Strafverfolgungsbehörden bei Verdacht auf Opioid-Überdosierung
- 19.11.2017 Opioid-Überdosis: Konzentriertes Naloxon-Nasenspray so gut wie Injektion
- 15.09.2017 EU: Opioidüberdosierung – CHMP-Zulassungsempfehlung
- 04.11.2016 Mundipharma gibt EU-Zulassungsantrag für Nyxoid bekannt
- Aug. 2012 Naloxon gegen Heroinsucht. Behandlung / Therapie der Abhängigkeit von Heroin und Morphium mit Naloxon erfolgreich
Mundipharma gibt EU-Zulassungsantrag für Nyxoid bekannt
04.11.2016 Mundipharma hat bei der Europäischen Arzneimittel-Agentur (EMA) einen Zulassungsantrag für Nyxoid (intranasales Naloxon 1,8 mg in 0,1 ml) eingereicht, der die Genehmigung für die Notfallumkehrung einer Opioid-Überdosis einholt.
Naloxon wird in routinemäßiger Praxis bereits seit über 40 Jahren verwendet, um die Auswirkungen von Opioid-Überdosierungen rückgängig zu machen, und ist in der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation (WHO) enthalten.
Eine intranasale Verabreichungsform wurde von Mundipharma entwickelt, um potentiellen „Ersthelfer“ in Überdosierungssituationen eine einfach zu bedienende, injektionsfreie Option zur Verfügung zu stellen, die für die Verwendung in einem Take-Home-Naloxon-Setting geeignet ist.
Der Zulassungsantrag von Mundipharma basiert auf Daten einer kürzlich durchgeführten 5-teiligen, offenen, randomisierten Einzeldosis-, Crossover-Studie mit 38 gesunden Probanden. Diese Studie zeigte, dass Nyxoid bioaquivalent zu injizierbarem Naloxon als Erstlinien-Behandlung bei Opioid-Überdosierung ist, wobei eine intranasale 1,8 mg-Dosis vergleichbar mit 0,4 mg intramuskulärem Naloxon ist, das derzeit als Standardbehandlung im Falle von Opioid-Überdosis gilt. Das Produkt ist gut verträglich mit einem ähnlichen Sicherheitsprofil wie das injizierbare Naloxon.
© arznei-news.de – Quelle: Mundipharma, Nov. 2016
EU: Opioidüberdosierung – CHMP-Zulassungsempfehlung
15.09.2017 Der Ausschuss für Humanarzneimittel der Europäischen Zulassungsbehörde (CHMP) empfiehlt die Zulassung von Nyxoid (aktive Substanz ist Naloxon) der Firma Mundipharma Corporation Limited als Nasenspray (1,8 mg) für die Behandlung von Opioidüberdosierung.
Der Nutzen des Medikaments ist seine Fähigkeit, Symptome der Opioidüberdosis umzukehren.
Die häufigsten Nebenwirkungen sind Übelkeit und Opioid-Entzugssyndrom.
Nyxoid ist ein Hybridmedikament von Naloxon HCl (Spritzenlösung), das seit 2006 in der EU zugelassen ist. Nyxoid enthält den gleichen Wirkstoff wie Naloxon HCl, wird aber in die Nasenlöcher verabreicht.
Kein Abo! (Schon ab 1,67€ für den Monat)
Indikation
Bei Zulassung wäre Nyxoid indiziert für die sofortige Verabreichung als Notfalltherapie bei bekannter oder vermuteter Opioid-Überdosierung, welche sich durch eine Depression der Atemwege und/oder des Zentralnervensystems manifestiert, sowohl im nicht-medizinischen als auch im medizinischen Bereich.
Das Medikament wäre bei Erwachsenen und Jugendlichen ab 14 Jahren indiziert.
Nyxoid ist kein Ersatz für die medizinische Notfallversorgung, schreibt die EMA.
© arznei-news.de – Quelle: EMA, Sept. 2017
Update: Das Medikament wurde für die obige Indikation in der EU zugelassen.
