Lungenerkrankungen – Herz-Kreislauf-Mittel
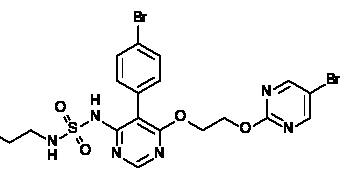
Macitentan ist ein oral wirksamer, dualer Endothelin Rezeptor-Antagonist, der bei pulmonaler arterieller Hypertonie eingesetzt wird. Handelsname ist Opsumit. Der ATC-Code ist C02KX04.
News
- 06.03.2023 Kombination Macitentan / Tadalafil bei pulmonaler arterieller Hypertonie von Nutzen. Daten der Phase-3-Studie A DUE zeigen, dass die Kombinationstherapie aus Macitentan und Tadalafil in Form einer Einzeltablette die pulmonale Hämodynamik bei Patienten mit pulmonaler arterieller Hypertonie (PAH) im Vergleich zu Monotherapien signifikant verbessert
- 23.10.2019 Neue Daten zu Macitentan zeigen Kombination mit Tadalafil verbessert hämodynamische klinische und funktionelle Parameter bei Patienten mit pulmonaler arterieller Hypertonie
- 19.09.2018 Portopulmonale Hypertonie – vielversprechende Resultate
- 2014 Jan.: Genehmigung für Vermarktung von Opsumit in der EU
- 2013 Okt.: Zulassung bei PAH durch die FDA.
Macitentan FDA-Zulassung: Pulmonale arterielle Hypertonie
Die U.S. Food and Drug Administration hat Opsumit (Wirkstoff Macitentan) für die Behandlung von Erwachsenen mit pulmonaler arterieller Hypertonie (PAH) genehmigt.
Pulmonale arterielle Hypertonie
Pulmonale arterielle Hypertonie ist eine chronische, fortschreitende und schwächende Krankheit, die zum Tod oder der Notwendigkeit einer Lungentransplantation führen kann.
Sicherheit und Wirksamkeit
Opsumits bzw. Macitentans Sicherheit und Wirksamkeit wurden in einer langfristigen klinischen Studie untersucht, in der 742 Teilnehmer zufällig Opsumit oder ein Placebo bekamen. Die durchschnittliche Behandlungsdauer war etwa zwei Jahre. In der Studie erwies sich Macitentan als wirkungsvoll bei der Verzögerung der Krankheitsprogression.
Wie andere Mitglieder seiner Medikamentenklasse trägt Opsumit die Warnung, dass das Medikament nicht bei schwangeren Frauen angewendet werden sollte, weil es den sich entwickelnden Fötus schaden kann.
Nebenwirkungen
Häufige Nebenwirkungen, die mit der Einnahme von Macitentan/Opsumit im Zusammenhang standen, waren:
- eine niedrige Anzahl roter Blutkörperchen (Anämie),
- erkältungsähnliche Symptome (Nasopharyngitis ),
- Halsschmerzen,
- Bronchitis,
- Kopfschmerzen,
- Grippe und
- Harnwegsinfektionen.
© arznei-news.de – Quelle: FDA, Okt. 2013
Opsumit – pulmonale arterielle Hypertonie
Update 05.02.2014: Zulassung bei pulmonale arterielle Hypertonie (PAH). Die EMA hat Opsumit (aktive Substanz Macitentan) genehmigt.
Opsumit ist als Monotherapie oder in Kombination für die langfristige Behandlung der pulmonalen arteriellen Hypertonie (PAH) bei erwachsenen Patienten der WHO-Funktionsklasse (FC) II bis III indiziert.
Zulassungsempfehlung Okt. 2013
Der Ausschuss für Humanarzneimittel der Europäischen Zulassungsbehörde (CHMP) hat auf seiner Oktober-Sitzung beschlossen, die Zulassung von Opsumit (Wirkstoff Macitentan) bei pulmonaler arterieller Hypertonie (PAH) zu empfehlen.
Opsumit von der Firma Actelion Registration Ltd soll für die Behandlung erwachsener PAH-Patienten der WHO-Funktionsklassen II und III als Mono- und Kombinationstherapie zugelassen werden.
Die aktive Substanz von Opsumit ist Macitentan, ein oral wirksamer, dualer Endothelin (ET) A und Endothelin B Rezeptor-Antagonist.
Nebenwirkungen
Die häufigsten Nebenwirkungen von Opsumit/Macitentan waren:
- Nasopharyngitis (14,0%),
- Kopfschmerzen (13,6%) und
- Anämie (13,2%).
Die meisten Nebenwirkungen sind leicht bis mittelschwer.
© arznei-news.de – Quelle: EMA, Okt. 2014
Portopulmonale Hypertonie – vielversprechende Resultate
19.09.2018 Actelion hat neue Daten einer randomisierten, kontrollierten klinischen Studie vorgestellt, in der Opsumit (Wirkstoff Macitentan) als potenzielle Behandlung der portopulmonalen Hypertonie (PoPH) ihr Hauptziel erreicht hat.
Portopulmonale Hypertonie
PoPH ist eine Untergruppe der pulmonalen arteriellen Hypertonie (PAH), die mit einem erhöhten Blutdruck in der Pfortader verbunden ist, oft aufgrund von Zirrhose.
Patienten mit der Erkrankung werden oft nur im Rahmen einer Beurteilung der Lebertransplantation diagnostiziert, schwere PAH ist jedoch aufgrund der schlechten postoperativen Prognose eine Kontraindikation für die Lebertransplantation.
Pulmonaler Gefäßwiderstand
Daten aus der Phase-III-Studie PORTICO, die auf dem Kongress der European Respiratory Society vorgestellt wurden, zeigen, dass Opsumit den pulmonalen Gefäßwiderstand (PVR) im Vergleich zu Placebo deutlich verbessert hat.
In der Studie wurden 85 Patienten im Verhältnis 1:1 in zwei Behandlungsgruppen randomisiert, und erhielten 10 mg Macitentan oder Placebo für eine 12-wöchige doppelblinde Behandlungsdauer.
Nach 12 Wochen Behandlung erreichte die Studie ihren primären Endpunkt, wobei sie eine Reduktion des pulmonalen Gefäßwiderstandes (PVR) für Macitentan um 35% im Vergleich zu Placebo zeigte.
Pulmonaler arterieller Druck
Macitentan verbesserte auch den mittleren pulmonalen arteriellen Druck (mPAP) und den Herzindex im Vergleich zu Placebo signifikant.
Darüber hinaus wurde kein signifikanter Unterschied zwischen Opsumit und Placebogruppen bei sechs Gehminuten (6MWD) oder der WHO-Funktionsklasse beobachtet.
Die häufigsten Nebenwirkungen waren periphere Ödeme und Kopfschmerzen.
Die Studie ergab auch, dass die Sicherheit von Opsumit ähnlich wie in früheren klinischen Studien zur portopulmonalen Hypertonie war.
© arznei-news.de – Quellenangabe: Actelion
Neue Daten zu Macitentan zeigen Kombination mit Tadalafil verbessert hämodynamische klinische und funktionelle Parameter bei Patienten mit pulmonaler arterieller Hypertonie
23.10.2019 Actelion Pharmaceuticals (zur Janssen Pharmaceutical Company gehörend) hat neue Daten zur Bewertung der ersten Kombinationstherapie von Opsumit (Wirkstoff Macitentan) und TadalafIl, einem PDE5-Hemmer, bekanntgegeben.
Patienten mit pulmonaler arterieller Hypertonie (PAH, WHO-Gruppe 1), die diese Kombination einnahmen, zeigten eine hämodynamische Verbesserung sowie Verbesserungen der Funktionsparameter und Risikoprofile.
Die Kombination wurde von diesen Patienten auch gut vertragen. Die Studiendaten wurden auf der CHEST-Jahrestagung 2019 veröffentlicht.
Die OPTIMA-Studie (COmbination theraPy of maciTentan and tadalafIl in patients with newly diagnososed pulMonary Arterial Hypertension) war eine prospektive, multizentrische, einarmige, offene Phase-IV-Studie zur Bewertung der Wirksamkeit, Sicherheit und Verträglichkeit der ersten oralen Kombinationstherapie von Opsumit und Tadalafil bei Patienten mit neu diagnostizierter PAH. Insgesamt wurden 46 Patienten in die Studie aufgenommen.
Sicherheit, Verträglichkeit, Nebenwirkungen
Die Sicherheits- und Verträglichkeitsergebnisse standen im Einklang mit früheren klinischen Studien, die die Zulassung und Anwendung von Opsumit 10mg einmal täglich unterstützten.
Die häufigsten unerwünschten Ereignisse (AE) in der OPTIMA-Studie waren peripheres Ödem (28,3%), Kopfschmerzen (23,9%), Durchfall (19,6%), Dyspnoe (15,2%), Anämie (13,0%) und Asthenie (13,0%).
Vier Patienten wiesen eine Abnahme des Hämoglobins unter 10 g/dl auf und ein Patient hatte Aminotransferasen ≥3 mal die Obergrenze des Normalen.
Drei Patienten brachen die Behandlung wegen Nebenwirkungen ab und drei Patienten starben während der Studie. Todesursachen waren Herzstillstand, Herzinsuffizienz und Multiorganversagen mit Sepsis.
© arznei-news.de – Quellenangabe: Actelion Pharmaceuticals / Janssen Pharmaceutical Company
Schreiben Sie uns >> hier << über Ihre Erfahrungen und lesen Sie die Erfahrungsberichte zu diesem Medikament.
