Kein Abo! (Schon ab 1,67€ für den Monat)
Zytokin-Hemmer gegen COVID-19 / Coronavirus
Mit Zytokin-Hemmern behandelte immunerkrankte Patienten zeigen keine Anzeichen einer Coronavirus-Infektion
Rituximab bei Neuromyelitis-optica-Spektrum-Erkrankungen
Sicherheit und Wirksamkeit von Rituximab bei Neuromyelitis-optica-Spektrum-Erkrankungen (NMOSD)
Siponimod (Mayzent)
Anhaltende Wirkung bei Patienten mit sekundär progredienter Multipler Sklerose (SPMS) um bis zu fünf Jahre durch Verzögerung der Behinderung
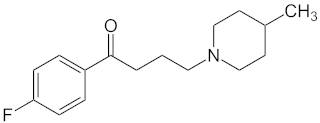
Melperon (Melneurin, Eunerpan)
Melperon wird vor allem bei Erregungs- und Spannungszuständen sowie Schlafstörungen eingesetzt.
Ravulizumab (Ultomiris) gegen COVID-19 / Coronavirus
Alexion berichtet über Pläne zur Einleitung einer Phase-3-Studie mit Ultomiris bei hospitalisierten Patienten mit schwerer COVID-19
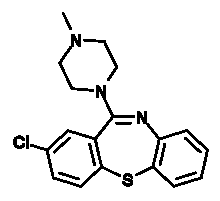
Clotiapin (Entumin)
Wirkstoff: Clotiapin; Wirkstoffklasse: Dibenzothiazepine
Wirkung auf Organismus: antipsychotisch. Es ist ein atypisches Antipsychotikum.
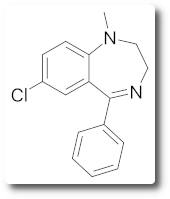
Medazepam (Rudotel)
Wirkung auf die Psyche: amnestisch, anxiolytisch, antikonvulsiv, sedierend und muskelrelaxierend. Das Medikament wird bei Angststörungen, Schlafstörungen eingesetzt.
Retigabin / Ezogabin bei Depression
Antiepileptikum Retigabin verringert deutlich die Symptome schwerer Depressionen
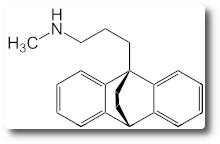
Maprotilin (Ludiomil)
Das Medikament wird bei depressiven Störungen aber auch bei Panikstörung, neuropathischen Schmerzen,
Bipolarer Depression,
zur symptomatischen Linderung von Ängsten