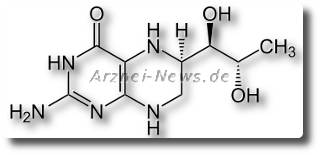
Sapropterin (Kuvan)
Update 21.07.2015 Zulassung in Europa für Kinder unter 4 Jahren * Sapropterin (Markenname Kuvan) oder 5,6,7,8-Tetrahydrobiopterin ist ein reduziertes Biopterin aus der chemischen Gruppe der Pterine und wird zur Behandlung von Hyperphenylalaninämie bei Patienten mit Phenylketonurie ...